Прогнозирование и профилактика атеросклеротических сердечно-сосудистых заболеваний
В начале XXI века казалось, что рак вытеснит болезни сердца с позиции главного убийцы человечества. Некоторые даже предсказывали, что спрос на кардиологов вскоре резко упадёт. Но прошло два десятилетия, и сегодня мы видим: сердечно-сосудистые заболевания по-прежнему в мире остаются ведущей причиной смерти [1].
Прогресс, достигнутый в кардиологии за последние полвека, действительно впечатляющ. Последние данные из многих стран указывают, что с 2019 года смертность от болезней сердца снова растёт (рис 1).
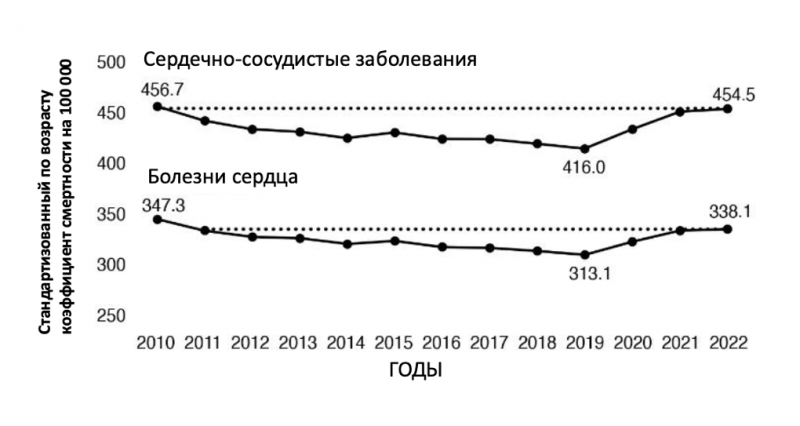
Рисунок 1. Недавний рост смертности от сердечно-сосудистых заболеваний, 2010–2022 гг. AAMR: скорректированный по возрасту коэффициент смертности. Адаптировано из Rebecca Woodruff et al., “Trends in cardiovascular disease mortality rates and excess deaths, 2010–2022,” American Journal of Preventive Medicine 66, no. 4 (April 2024): 582–89, https://doi.org/10.1016/j.amepre.2023.11.009.
Что же пошло не так?
Причины прежнего успеха были хорошо известны: значительное снижение курения, массовое использование статинов, лучший контроль артериального давления, а также современные методы восстановления кровоснабжения миокарда — как при остром инфаркте, так и в плановом порядке с помощью шунтирования или стентирования. Кроме того, совершенствование лечения сердечной недостаточности и аритмий позволило продлить жизнь миллионам пациентов [2,3].
Однако определить точные причины разворота этой благоприятной тенденции не так просто.
Среди главных подозреваемых — эпидемия ожирения и диабета. Вероятно, свою роль сыграло и ухудшение поведенческих привычек: малоподвижный образ жизни, некачественное питание, хронический стресс и загрязнение окружающей среды. Ирония в том, что в отличие от большинства других болезней старения, до 90% случаев сердечно-сосудистых заболеваний можно предотвратить — с помощью простых изменений образа жизни [4].
Сердечно-сосудистые заболевания — это, возможно, самый предотвратимый из всех хронических убийц, с которыми сталкивается современное общество. Но, несмотря на знание, инструменты и предупреждения, мы снова сдаём позиции.
И это требует осмысления.
ЭКСПЕРТНЫЙ ВЗГЛЯД НА АТЕРОСКЛЕРОЗ
Атеросклероз — основная причина болезней сердца и сосудов. Название этого состояния происходит от греческих слов athero («каша» или «похлёбка») и skleros(«твёрдый»), что в буквальном смысле можно перевести как «затвердевшая каша». Чтобы представить себе этот образ, достаточно сварить овсянку и оставить кастрюлю немытой на несколько часов: засохшая масса на стенках — яркая аналогия тому, что происходит внутри наших артерий.
Термин «атеросклероз» был введён немецким патологом Феликсом Маршаном в 1904 году. Он использовал его для описания жироподобного вещества, которое обнаруживал внутри артерий. Сегодня его называют атеросклеротической бляшкой. Она формируется из-за накопления липопротеинов низкой плотности (ЛПНП) и других липидных частиц — сложных молекул, переносящих холестерин в составе белково-жировых комплексов.
Бляшки накапливаются годами. Процесс начинается с проникновения ЛПНП в стенку артерии и сопровождается хроническим воспалением. Исход атеросклероза может быть разным. Иногда всё происходит внезапно — когда бляшка трескается или разрывается, формируется тромб, и это становится непосредственной причиной инфаркта. В других случаях заболевание развивается постепенно, и артерия сужается настолько, что кровоток к сердцу ограничивается, хотя и не прекращается полностью.
Основными факторами, усиливающими развитие атеросклероза, являются курение, неконтролируемая гипертония, сахарный диабет (вместе с хронически повышенным уровнем глюкозы) и аномальный липидный профиль крови — прежде всего высокий уровень ЛПНП [5, 6].
Современные исследования всё чаще описывают атеросклероз как опухолеподобный процесс: ключевую роль в нём играют гладкомышечные клетки сосудистой стенки [7,8]. Отмечены параллели между факторами риска рака и сердечно-сосудистых заболеваний — от образа жизни до системного воспаления [9,10]. Добавим к этому и аутоиммунный компонент: у людей с аутоиммунными заболеваниями риск инфаркта и инсульта существенно выше [11,12].
Хотя ишемическая болезнь сердца обычно диагностируется в пожилом возрасте, сам процесс атерогенеза начинается намного раньше. Уже у подростков и молодых людей можно обнаружить начальные атеросклеротические изменения. По данным внутрисосудистого ультразвукового исследования, к 30 годам большинство людей имеют те или иные признаки раннего поражения коронарных артерий (см. рис. 2)
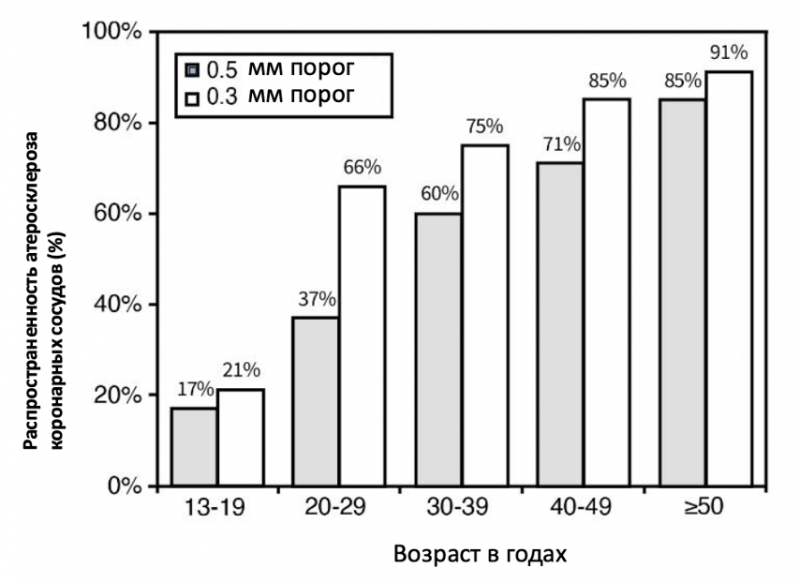
Рисунок 2. Распространённость коронарного атеросклероза у молодых людей в зависимости от порогов поражения сосудов. Источник: EM Tuzcu et al., “High Prevalence of Coronary Atherosclerosis in Asymptomatic Teenagers and Young Adults: Evidence From Intravascular Ultrasound,” Circulation 103, no. 22 (June 2001): 2705–10. https://doi.org/10.1161/01.cir.103.22.2705
Чем раньше в жизни будут устранены факторы риска — курение, неправильное питание, малоподвижность и другие, — тем меньше вероятность накопления значительных атеросклеротических бляшек и их осложнений. Это ключевой момент в понимании всех возрастных заболеваний — сердца, мозга и онкологии: клинически они проявляются спустя десятилетия, но формироваться начинают задолго до этого. Именно в этом — уникальное окно возможностей для профилактики.
СКРЫТАЯ УГРОЗА: КАК АТЕРОСКЛЕРОЗ РАЗВИВАЕТСЯ БЕЗ СИМПТОМОВ
Одно из крупнейших проспективных исследований, проведённое в Дании, проанализировало состояние коронарных артерий у более чем 9500 человек в возрасте от 40 лет и старше, у которых не было симптомов или известных сердечно-сосудистых заболеваний. Участникам провели компьютерную томографию (КТ) коронарных артерий, а затем наблюдали за ними в течение трёх с половиной лет [13].
Результаты оказались поразительными: примерно у половины обследованных не было признаков атеросклероза. У остальных заболевание варьировалось по степени и распространённости (см. рис. 3). Выяснилось, что:
• Обструктивная или обширная ишемическая болезнь сердца увеличивала риск инфаркта в 8–9 раз;
• Если одновременно присутствовали и обструкция, и обширность поражения, риск возрастал в 13 раз;
• Даже необструктивный, но обширный атеросклероз несли тройной риск инфаркта;
• Повышенный риск смерти или инфаркта наблюдался во всех группах с проявлениями заболевания.
Даже за такой короткий срок наблюдения стало очевидно: субклинический атеросклероз представляет серьёзную опасность. Эти данные подчёркивают высокую распространённость ишемической болезни сердца среди людей без каких-либо симптомов. Это и есть главная причина важности раннего скрининга. Представьте, какую пользу принесло бы знание о том, кто находится в группе риска, ещё до появления первых признаков болезни — и без необходимости проводить КТ всем подряд.
Американская кардиологическая ассоциация выделяет восемь ключевых факторов, определяющих сердечно-сосудистое здоровье: сбалансированное питание, регулярная физическая активность, отказ от курения, здоровый сон, нормальный вес, стабильные уровни холестерина, сахара и артериального давления. Все они — основные движущие силы в развитии атеросклероза. Но не стоит забывать и о генетике. Пусть и нечасто, но встречаются случаи, когда сердечные приступы случаются у людей без гипертонии, диабета или нарушений липидного обмена — иногда это единственный звоночек генетической предрасположенности [14].
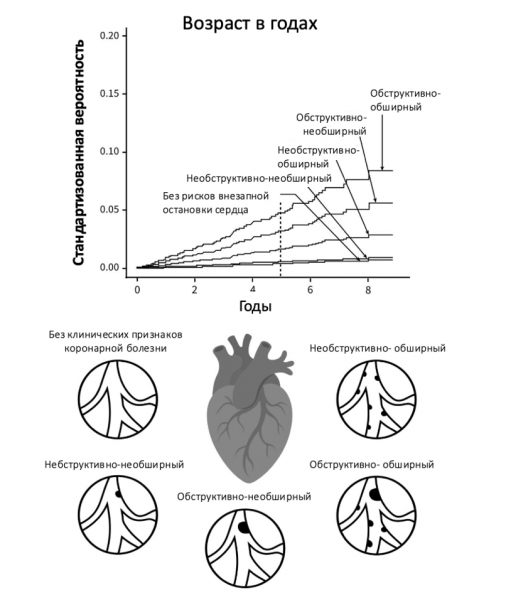
Рисунок 3. Риск инфаркта миокарда в зависимости от характера атеросклеротического поражения коронарных артерий — обструктивное или необструктивное, обширное или ограниченное. Источник: Andreas Fuchs et al., “Subclinical Coronary Atherosclerosis and Risk of Myocardial Infarction in the Copenhagen General Population Study,” Annals of Internal Medicine 176, no. 4 (2023): 433–42.
Около 5% пациентов с коронарной болезнью сердца сталкиваются с ней в возрасте до 40–45 лет — так называемая преждевременная ИБС. У 60% из них при этом отсутствует семейный анамнез. Здесь особенно полезны полигенные показатели риска — инструменты, которые помогают выявлять унаследованную предрасположенность к заболеванию [15,16].
Такие подходы уже внедряются в ряде медицинских систем США, включая MassGeneral Brigham, и используются рядом страховых компаний. Полигенные тесты становятся всё более доступными через коммерческие сервисы — Genetype, GenomicPLC, Open DNA, Ambry Genetics, Myriad Genetics и Haplotype Labs. Например, среди пациентов Mass General Brigham, вошедших в верхние 10% по полигенному риску, вероятность развития сердечно-сосудистых заболеваний была в два раза выше в среднем, а среди людей азиатского происхождения — почти в четыре раза выше [17,18].
Эти данные были подтверждены в крупном исследовании, финансируемом Национальными институтами здоровья США (NIH), где высокий риск определялся как попадание в верхние 5% по полигенному показателю. Среди более чем 2500 человек, чьи риски оценивались по 10 различным полигенным шкалам, ишемическая болезнь сердца оказалась заболеванием с наибольшей прогностической значимостью [19,20].
Аналогичное проспективное исследование в Китае, охватившее более 96 тысяч участников, подтвердило: сочетание полигенного риска и факторов образа жизни оказывает аддитивное влияние на вероятность развития сердечно-сосудистых заболеваний. Это открывает путь к персонализированной профилактике — когда вмешательство можно начинать задолго до появления первых симптомов [21].
НОВАЯ ЭРА ПРОФИЛАКТИКИ: ГЕНЫ, БЕЛКИ И МИКРОБИОМ В ОЦЕНКЕ СЕРДЕЧНО-СОСУДИСТОГО РИСКА
Идеальный сценарий профилактики — это знание своего сердечно-сосудистого риска с раннего возраста. Особенно важно понимать, что полигенный показатель риска (набор наследуемых генетических вариаций) действует независимо от традиционных факторов, включая семейный анамнез, и дополняет их. Люди с высоким полигенным риском чаще всего выигрывают от раннего назначения статинов, что делает генетическое тестирование важным шагом к первичной профилактике ишемической болезни сердца — особенно если оно проводится в молодом возрасте.
Кроме того, осознание принадлежности к группе высокого риска способно изменить поведение человека. В клинической практике важно использовать полигенные показатели, чтобы принимать решение о целесообразности назначения статинов пациентам с минимальными или отсутствующими традиционными факторами риска.
Тем не менее, на сегодняшний день генетическая оценка ещё не стала частью рутинной клинической практики.
БЕЛКИ КАК МАРКЕРЫ РИСКА
Помимо генетики, значимыми индикаторами риска выступают белки плазмы крови. Протеомный анализ — оценка набора белков в организме — предлагает дополнительный уровень диагностики. В исследовании UK Biobank, охватившем более 22 тысяч человек, уровень более 300 белков оказался тесно связан не только с сердечно-сосудистым, но и с общесистемным риском заболеваний. Эта оценка эффективно дополняла полигенный риск и, что особенно важно, могла быть модифицирована с помощью физических упражнений [22].
Созданы и так называемые «протеомные часы сердца», построенные на анализе примерно 850 белков. Они прошли валидацию в нескольких популяционных когортах и выявили, что около 2% людей демонстрируют ускоренное старение сердца — потенциально применимое в клинической практике для раннего выявления риска [23,24].
Интересно, что непосредственный риск инфаркта в течение ближайших шести месяцев удалось предсказать с высокой точностью, если к стандартной клинической информации добавлялись данные о 48 белках и 43 метаболитах в крови [25].
КЛОНАЛЬНЫЙ ГЕМОПОЭЗ И ЕГО РОЛЬ
С возрастом кроветворные стволовые клетки могут накапливать определённые мутации — явление, известное как клональный гемопоэз неопределённого потенциала (CHIP). Несмотря на название, этот процесс далеко не безобиден: наличие CHIPдостоверно связано с повышенным риском сердечно-сосудистых заболеваний и тромбозов. У людей старше 70 лет он увеличивает риск ССЗ более чем в шесть раз. Несмотря на это, ни один из этих белковых или генетических маркеров пока не интегрирован в стандартную медицинскую практику [26, 27].
МИКРОБИОМ: НОВЫЙ ГОРИЗОНТ ПРОФИЛАКТИКИ
Ещё дальше от клинической практики — но не менее перспективен — микробиом кишечника как показатель риска сердечно-сосудистых заболеваний. В масштабном исследовании с участием около 5000 человек, наблюдаемых на протяжении 18 лет, включение микробиомного индекса в модель оценки риска (наряду с клиническими и генетическими данными) дало вклад, сопоставимый по значимости с такими параметрами, как артериальное давление, уровень холестерина и триглицериидов [28,29].
Отдельный анализ микробиома у 1400 участников выявил специфические бактерии, способные метаболизировать холестерин и снижать его уровень в крови. Это ещё раз подтверждает, что микробиом играет активную роль в регуляции сердечно-сосудистого здоровья [30,31].
Особенно интересным оказалось наблюдение за так называемым метаболическим возрастом кишечника. У пожилых людей наличие определённых микробов, например низкий уровень Prevotella, ассоциировалось с пониженным риском сердечно-сосудистых заболеваний — даже несмотря на возраст [32,33].
Кроме того, в исследовании микробиома более 57 тысяч человек из 32 стран выяснилось, что наличие одноклеточного организма Blastocystis коррелировало с лучшим метаболическим профилем, меньшим ожирением и лучшими кардиометаболическими исходами. Его распространённость возрастала у людей, придерживающихся здоровой диеты [34,35].
Эти наблюдения укрепляют представление о том, что комплексная оценка риска — генетическая, протеомная и микробиомная — открывает новые возможности в профилактике возрастных заболеваний. Мы всё ближе к тому, чтобы управлять не только болезнью, но и её вероятностью — задолго до появления первых симптомов.
КАЛЬЦИЕВЫЙ ИНДЕКС: ПОЛЬЗА, ОГРАНИЧЕНИЯ И МИФЫ
Гораздо более широкое распространение в клинической практике получил кальциевый индекс, рассчитываемый на основе компьютерной томографии. Этот метод оценивает накопление кальция в коронарных артериях, которое может, но не обязательно должно сопровождаться наличием атеросклеротической бляшки. Поэтому кальциевый индекс — это непрямой маркер, отражающий отложение кальция в стенках артерий, а не саму степень сужения просвета сосуда.
Несмотря на определённую диагностическую ценность, этот тест часто чрезмерно используется — особенно у людей без выраженных факторов риска. Его даже рекламируют как «романтичный подарок» ко Дню святого Валентина. Часто к этому методу направляют пациентов после выявления индекса выше 100, которые находятся в тревоге, считая себя в группе высокого риска фатального инфаркта. На деле же клинически значимым считается кальциевый индекс, превышающий 300, и только в этом диапазоне он действительно коррелирует с повышенным риском сердечно-сосудистых событий. Более низкие значения требуют контекстуального анализа, а не паники [36,37].
Почти сорок лет спустя после внедрения теста на кальциевый индекс, только недавно начались рандомизированные клинические исследования, призванные ответить на главный вопрос: влияет ли знание результатов этого теста на долгосрочные исходы для пациентов?
Отдельного внимания заслуживает КТ сердца с контрастированием, которая позволяет более точно визуализировать внутреннюю структуру артерий и выявлять воспаление — ключевой механизм развития атеросклероза.
ЛЕКАРСТВЕННАЯ ТЕРАПИЯ: АГРЕССИВНОЕ СНИЖЕНИЕ ЛПНП КАК СТРАТЕГИЯ ПРОФИЛАКТИКИ
Задолго до появления кальциевого индекса или полигенных показателей риска, липопротеины низкой плотности (ЛПНП) — так называемый «плохой» холестерин — уже были признаны ключевым биомаркером сердечно-сосудистого риска. Это один из самых изученных лабораторных показателей в современной медицине. Многочисленные крупные рандомизированные клинические исследования статинов подтвердили прямую зависимость между уровнем ЛПНП и частотой сердечно-сосудистых событий. На рисунке 4 каждая точка представляет отдельное исследование, наглядно демонстрируя: чем ниже уровень ЛПНП, тем меньше риск ишемической болезни сердца.
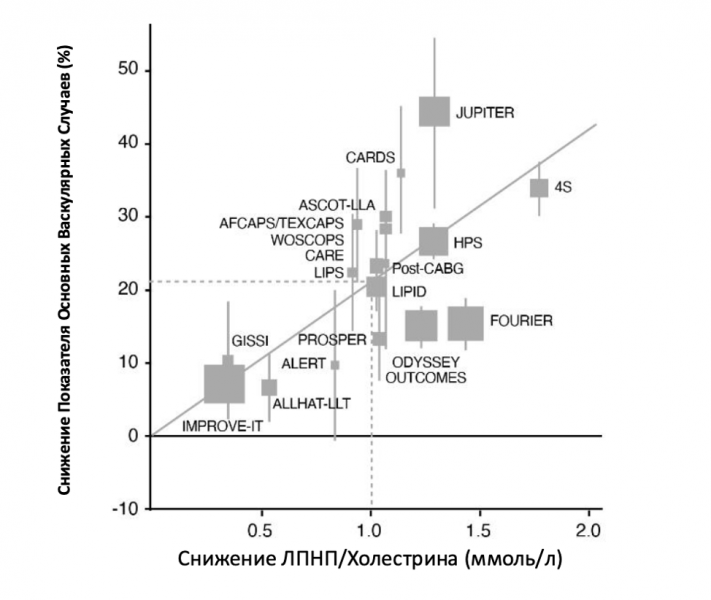
Рисунок 4. Снижение уровня холестерина ЛПНП в различных рандомизированных исследованиях и снижение частоты серьезных сердечно-сосудистых событий. Названия исследований являются акронимами. Адаптировано из FB Mensink et al., “Pharmaco-invasive therapy: Early implementation of statins and proprotein convertase subtilisin/kexin type 9 inhibitors after acute coronary syndrome,” Frontiers in Cardiovascular Medicine 9 (декабрь 2022): 1061346, https://doi.org/10.3389/fcvm.2022.1061346.
В последние годы укрепляется парадигма так называемой «гонки ко дну» — агрессивного снижения ЛПНП до очень низких значений, вплоть до менее 50 мг/дл, а в ряде случаев и ниже [38,39]. Это стало возможным благодаря расширению арсенала гиполипидемических средств:
• Статины (основа терапии),
• Эзетимиб (Зетия) — препарат, снижающий всасывание холестерина,
• Бемпедоевая кислота (Некслетол) — пероральное средство нового поколения,
• Ингибиторы PCSK9 — инъекционные препараты, блокирующие ключевой белок в метаболизме холестерина (алирокумаб [Пралуент], эволокумаб [Репата]),
• Инклисиран (Легио) — инновационный препарат на основе малых интерферирующих РНК, вводимый раз в шесть месяцев.
Таблица 2. Различные классы лекарств от атеросклероза
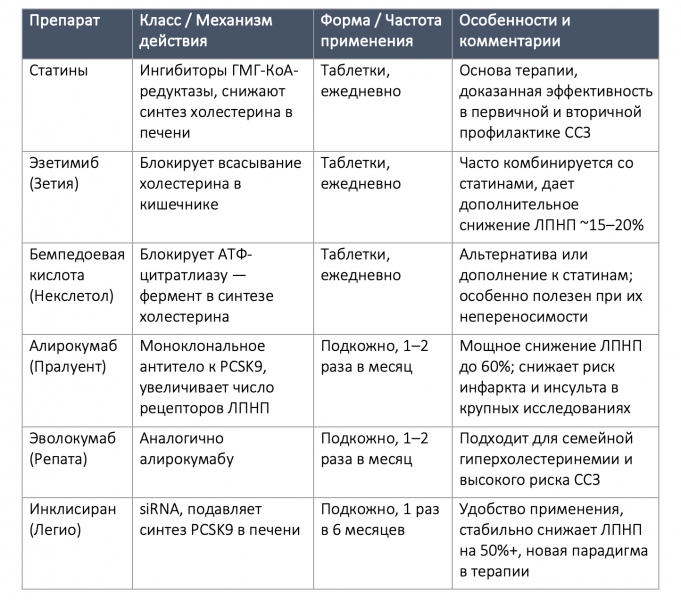
Хотя окончательно оптимальный целевой уровень ЛПНП всё ещё не определён, у пациентов с уже диагностированной ишемической болезнью сердца целесообразно стремиться к уровню ниже 50 мг/дл, при условии хорошей переносимости терапии. Некоторые клиницисты даже выступают за снижение до почти нулевых значений у пациентов с изолированно повышенным ЛПНП, но без других факторов риска — полагая, что это может продлить жизнь. Хотя такие предположения пока не подтверждены долгосрочными данными, общее направление исследований и клинической практики однозначно движется в сторону более раннего и более интенсивного лечения [40,41].
Дополнительные аргументы в пользу агрессивной стратегии появились после анализа недавнего исследования у пациентов со стабильной ишемической болезнью сердца, где достижение уровней ЛПНП ниже 20 мг/дл сопровождалось значительным снижением риска инфаркта, инсульта и сердечно-сосудистой смертности, что укрепляет эту цель как обоснованную стратегию вторичной профилактики (см. рис. 5).
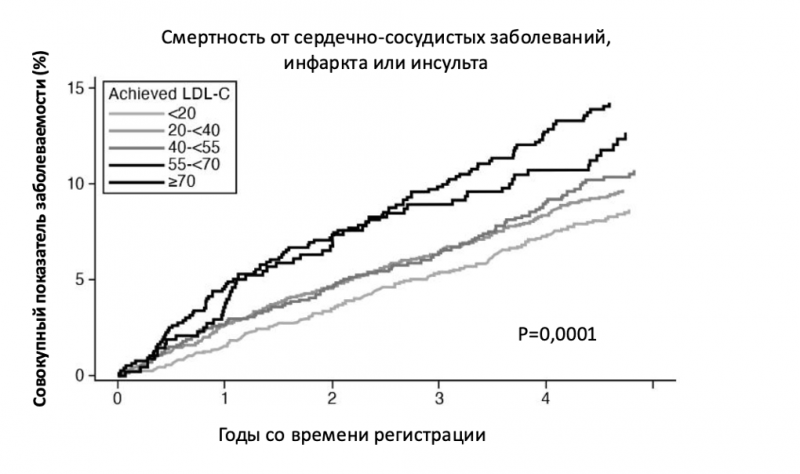
Рисунок 5. Абсолютный достигнутый уровень холестерина ЛПНП и снижение триады сердечно-сосудистой смерти, инфаркта миокарда (ИМ) и инсульта. Адаптировано из Prakriti Gaba et al., “Association between achieved low-density lipoprotein cholesterol levels and long-term cardiovascular and safety outcomes: An analysis of fourier-ole,” Circulation 147, no. 16 (апрель 2023): 1192–203
Важно помнить и о потенциальных побочных эффектах, в частности, повышенном риске развития сахарного диабета 2 типа при использовании высоких доз статинов. Этот эффект был выявлен в ряде исследований, включая рандомизированное сравнение розувастатина и аторвастатина, а также в метаанализах. Тем не менее, у пожилых пациентов имеются убедительные данные в пользу безопасности и эффективности статинов [42,43].
ДРУГИЕ ЛИПИДНЫЕ МАРКЕРЫ И НОВЫЕ ПОДХОДЫ К ЛЕЧЕНИЮ ГИПЕРТРИГЛИЦЕРИДЕМИИ
Помимо ЛПНП, существует ряд других лабораторных показателей, отражающих липидный профиль и помогающих в оценке сердечно-сосудистого риска. В стандартной липидной панели обычно определяются триглицериды и липопротеины высокой плотности (ЛПВП). Повышенные уровни триглицеридов натощак в сочетании с низким уровнем ЛПВП часто свидетельствуют о инсулинорезистентности и повышенном кардиометаболическом риске.
Существует прямая зависимость между уровнем триглицеридов и риском сердечно-сосудистых событий. Хотя умеренное повышение триглицеридов, как правило, хорошо поддаётся коррекции при снижении веса и изменении образа жизни, у лиц с высоким риском и недостаточным ответом на немедикаментозные меры может рассматриваться лекарственная терапия [44,45].
Одним из таких препаратов является икозапент этил (Васцепа) — очищенная и модифицированная форма эйкозапентаеновой кислоты (одного из компонентов рыбьего жира). Он получил одобрение на основании крупного клинического исследования, показавшего снижение сердечно-сосудистых событий. Однако результаты остаются предметом дискуссий, поскольку другие исследования с применением омега-3 жирных кислот не продемонстрировали аналогичного эффекта [46,47].
Также развивается направленная терапия высокой гипертриглицеридемии:
• Олизарсен — препарат, способный снижать уровень триглицеридов на 50% при ежемесячном введении,
• РНК-интерференционные препараты, нацеленные на ключевые гены липидного обмена — ANGPTL3 и APOC3, — позволяют достичь глубокого снижения триглицеридов у пациентов с резистентными формами дислипидемии.
Таблица 2. Лекарства от атеросклероза
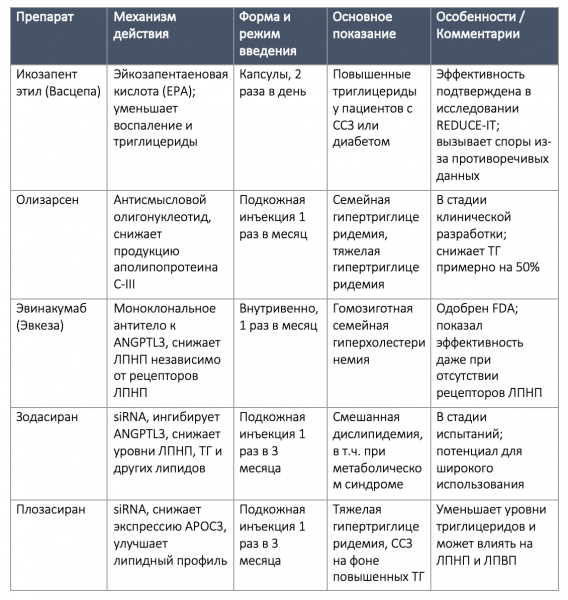
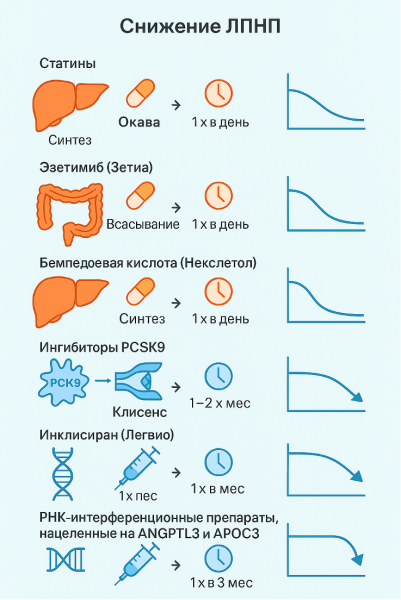
Рисунок 6. Механизмы действия лекарств от атеросклероза
Особого внимания заслуживают пациенты с семейной гиперхолестеринемией, особенно при наличии двух копий мутантных генов, поскольку они подвержены экстремально высокому риску атеросклероза уже в молодом возрасте. Для таких пациентов одобрен препарат эвинакумаб (Эвкеза) — моноклональное антитело к ANGPTL3, показавшее эффективность даже у детей с этим редким, но тяжёлым заболеванием [48,49].
Перспективные молекулы — зодасиран (направлен на ANGPTL3) и плозасиран (направлен на APOC3) — вводятся раз в три месяца и обладают широким положительным эффектом на липидный профиль, что делает их потенциально особенно ценными при смешанных типах дислипидемии [50-51].
ЛИПОПРОТЕИНЫ И РАСШИРЕННАЯ ЛИПИДНАЯ ДИАГНОСТИКА: НОВЫЕ АКЦЕНТЫ В КАРДИОМЕТАБОЛИЧЕСКОЙ ОЦЕНКЕ
Связь между липопротеинами высокой плотности (ЛПВП), часто называемыми «хорошим холестерином», и сердечно-сосудистыми исходами принципиально отличается от роли ЛПНП или триглицеридов. В отличие от них, ЛПВП сегодня всё чаще рассматриваются не как активные участники процесса атерогенеза, а скорее как маркеры, сопровождающие другие метаболические изменения. Более того, парадоксальные данные свидетельствуют: очень высокие уровни ЛПВП (более 80 мг/дл) могут быть связаны с повышенным общим и сердечно-сосудистым риском. Это может отражать наличие дисфункциональных частиц ЛПВП, которые не выполняют свою предполагаемую роль — транспортировать избыток холестерина обратно в печень [52,53].
Как и в случае с высокими триглицеридами, низкие уровни ЛПВП (<40 мг/дл у мужчин и <50 мг/дл у женщин) часто являются отражением инсулинорезистентности и хорошо поддаются коррекции с помощью изменения образа жизни. Однако, в отличие от убедительных данных о пользе снижения ЛПНП, активные попытки повысить ЛПВП или снизить триглицериды не привели к убедительным улучшениям клинических исходов в рандомизированных исследованиях. Тем не менее, хорошая липидограмма по-прежнему имеет значение в общей оценке сердечно-сосудистого риска [54,55].
ЛИПОПРОТЕИН(А): НЕУЧТЁННЫЙ, НО ЗНАЧИМЫЙ ФАКТОР РИСКА
Один из наиболее недооценённых липидных маркеров — липопротеин(а) или Лп(а). Несмотря на то что повышенные уровни Лп(а) однозначно ассоциированы с сердечно-сосудистыми заболеваниями, менее 0,5% пациентов проходят тестирование. Новые препараты, включая пероральные средства, уже демонстрируют снижение Лп(а) на 65% в ранних испытаниях, а также ведутся активные разработки интерферирующих РНК и других биологических препаратов, нацеленных на подавление синтеза Лп(а). Если они окажутся эффективными, тест на Лп(а) вполне может стать частью рутинной липидограммы [56,57].
АПОЛИПОПРОТЕИН B (АПОВ): НАДЁЖНЫЙ ИНДИКАТОР РИСКА
Другой важный, но часто недооценённый показатель — аполипопротеин B (апоВ). Хотя он тесно коррелирует с уровнем ЛПНП, апоВ является более точным предиктором риска, поскольку отражает общее количество атерогенных липопротеиновых частиц: ЛПНП, ЛППП, ЛПОНП и Лп(а). У примерно 20% людей с нормальным уровнем ЛПНП может быть повышен апоВ, что указывает на скрытый риск атеросклероза [59,60].
Учитывая его информативность, апоВ должен быть включён в стандартные липидные панели, особенно для пациентов с метаболическим синдромом, гипертриглицеридемией или высоким полигенным риском. Пока это не стало реальностью, альтернативой может служить расчет не-ЛПВП-холестерина (общий холестерин минус ЛПВП). Хотя это суррогатный показатель, он хорошо коррелирует с апоВ и может использоваться как вспомогательный ориентир [61,62].
Таким образом, современный взгляд на липидный профиль выходит за рамки простого измерения ЛПНП. Расширенное тестирование — на апоВ и Лп(а) — должно стать стандартом у пациентов с повышенным риском, поскольку именно эти маркеры позволяют выявить «скрытые» формы дислипидемии и точно нацелить терапию.
Хорошая новость — на горизонте появляются новые препараты для лечения аномальных липидов, прежде всего биологические малые интерферирующие РНК, направленные на специфические гены — технология, которая ранее казалась невозможной. Это полностью меняет подходы не только к скринингу, но и к терапии пациентов из группы высокого риска. Кроме того, есть эффективные альтернативы для тех, кто плохо переносит статины — например, бемпедоевая кислота и несколько блокаторов PCSK9.
Хотя контроль липидных нарушений является краеугольным камнем профилактики атеросклероза, не менее важен тщательный контроль гипертонии и диабета, если они присутствуют. Эти факторы риска тесно взаимосвязаны, ведь здоровье сердечно-сосудистой системы напрямую влияет на кровоснабжение всех органов. Помимо этой прямой взаимосвязи, существует значительное перекрытие факторов риска, влияющих на различные системы организма.
ВОСПАЛЕНИЕ, КАК ВАЖНЫЙ ФАКТОР СЕРДЕЧНО-СОСУДИСТЫХ ЗАБОЛЕВАНИЙ
С появлением убедительных данных о том, что воспаление лежит в основе атеросклероза, а высокочувствительный С-реактивный белок (вч-СРБ) служит маркером системного воспаления, был заложен фундамент для клинических испытаний. Они ставили целью проверить гипотезу: может ли мощный противовоспалительный препарат снизить риск сердечно-сосудистых заболеваний?
В 2017 году было опубликовано исследование CANTOS (Canakinumab Anti-inflammatoryThrombosis Outcome Study), в котором приняли участие более десяти тысяч пациентов с перенесённым инфарктом и повышенным уровнем вч-СРБ. Их случайным образом разделили на три группы, получавшие разные дозы канакинумаба — моноклонального антитела к интерлейкину-1β — или плацебо каждые три месяца на протяжении почти четырёх лет [63,64].
При более высоких дозах препарат снижал уровень вч-СРБ на 40% и, что особенно важно, без изменения липидного профиля значительно уменьшал число инфарктов, инсультов и сердечно-сосудистой смертности. Однако у небольшой части пациентов (около 0,3% по сравнению с 0,18% в группе плацебо) наблюдалось увеличение смертельных инфекций и случаев сепсиса, что связано с иммуносупрессивным эффектом препарата. Ещё одним важным открытием стало значительное снижение смертности от рака, в частности рака лёгких [65,66].
Таким образом, мощный противовоспалительный препарат одновременно подавлял сердечно-сосудистые события и снижал риск онкологических заболеваний — при этом риск смертельных инфекций оставался низким, но заметным. Несмотря на эти впечатляющие результаты, производитель, компания Novartis, решил не продвигать препарат для показания в кардиологии.
КОЛХИЦИН В КАРДИОЛОГИИ: ДРЕВНЕЕ СРЕДСТВО С НОВЫМ НАЗНАЧЕНИЕМ
Еще одна попытка решить проблему воспаления при сердечно-сосудистых заболеваниях была предпринята с применением колхицина — мощного противовоспалительного средства, известного человечеству более трёх тысяч лет и выделенного в XIX веке. В отличие от дорогостоящих моноклональных антител, колхицин доступен по цене и принимается перорально. Его основные побочные эффекты связаны с желудочно-кишечным трактом, прежде всего диареей, которая возникает примерно у каждого четвёртого пациента.
В рандомизированном исследовании, включавшем почти пять тысяч пациентов в первые тридцать дней после инфаркта миокарда с двухлетним наблюдением, группа, принимавшая колхицин, продемонстрировала значительное снижение сердечно-сосудистых событий по сравнению с плацебо — абсолютная польза составила примерно двух человек на сто. Как и в исследовании CANTOS, здесь отмечался несколько повышенный риск инфекций, преимущественно пневмонии, чаще встречавшейся среди пациентов, принимавших колхицин [66,67].
Дальнейшее крупное рандомизированное исследование с участием более пяти тысяч пациентов с хронической ишемической болезнью сердца выявило снижение сердечно-сосудистых событий на 30% (польза почти для трёх из ста человек), однако отмечено небольшое увеличение смертей, не связанных с сердечно-сосудистыми причинами — примерно два случая на тысячу [68,69].
В совокупности данные трёх исследований убедительно доказывают, что противовоспалительная терапия способна снизить риск инфарктов, инсультов и сердечно-сосудистой смертности. В июне 2023 года FDA одобрило версию колхицина (0,5 мг) под названием Lodoco как первый препарат для лечения сердечно-сосудистого воспаления. Однако несмотря на убедительные данные, подтверждённые метаанализом пяти рандомизированных исследований (см. рисунок 7), ни один из этих препаратов пока не вошёл в рутинную клиническую практику. Объединённый анализ показал отсутствие значимого увеличения риска инфекций или пневмонии. В 2024 году дополнительное шестое рандомизированное исследование у пациентов с перенесённым инсультом вновь подтвердило эффективность колхицина.
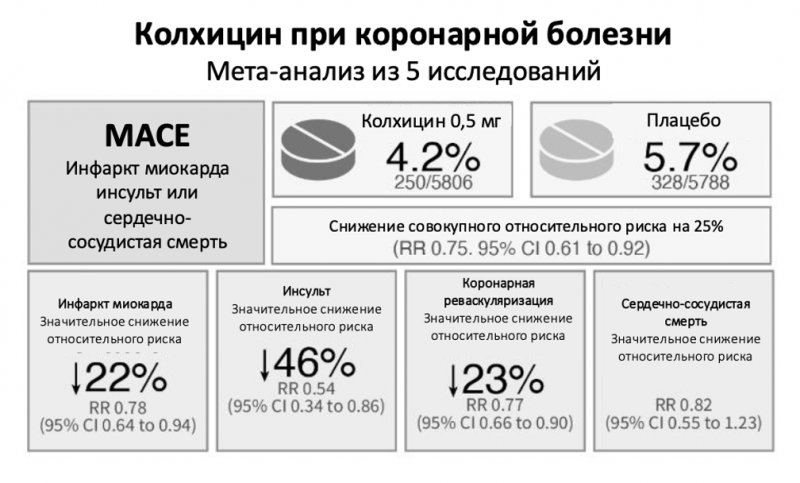
Рисунок 7. Резюме результатов пяти рандомизированных исследований колхицина при ишемической болезни сердца. Адаптировано из Aernoud Fiolet et al., “Efficacy and safety of low-dose colchicine in patients with coronary disease: A systematic review and meta-analysis of randomized trials,” European Heart Journal 42, no. 28 (July 2021): 2765–75
ДИАГНОСТИКА И ЛЕЧЕНИЕ УЯЗВИМЫХ БЛЯШЕК: ПАРАДИГМА СМЕЩАЕТСЯ
Существует важный способ оценки воспаления коронарных артерий — КТ-коронарная ангиография позволяет определить степень воспаления жировой ткани, окружающей каждую из трёх основных коронарных артерий. В исследовании с участием более 40 тысяч человек, из которых подгруппа наблюдалась почти восемь лет, более 80% не имели обструктивного коронарного заболевания, то есть значительного атеросклеротического сужения. Тем не менее, у этой группы наблюдался существенно повышенный риск серьёзных неблагоприятных событий — более 60% всех серьёзных сердечно-сосудистых исходов. В расширенной когорте была обнаружена поразительная связь между степенью воспаления артерий и риском осложнений. Например, при воспалении всех трёх артерий риск сердечно-сосудистой смерти был в 30 раз выше, а при воспалении одной артерии — в 13 раз выше, по сравнению с отсутствием воспаления, что значительно превосходит традиционные методы оценки клинических факторов риска (см. рисунок 8).
Существует также возможность более прямого выявления высокорисковых, так называемых уязвимых бляшек в коронарных артериях — даже при отсутствии значительного сужения или ограничения кровотока. В рандомизированном исследовании с участием 1600 пациентов с такими бляшками сравнивали два подхода: инвазивное лечение (баллонная ангиопластика или стентирование) и медикаментозную терапию. В ходе двухлетнего наблюдения группа, получавшая вмешательство, показала существенное снижение числа серьёзных сердечно-сосудистых событий. Эти результаты поставили под сомнение традиционное представление о том, что стентирование необходимо лишь при выраженном сужении артерий — так называемых «закупорках».
Объединяя данные всех этих исследований, можно уверенно утверждать: системное и локальное воспаление коронарных артерий — значимый фактор риска серьёзных сердечно-сосудистых событий, и противовоспалительная терапия способна улучшать прогноз пациентов. Тем не менее, несмотря на эти убедительные доказательства и возможности диагностики воспаления, кардиологическое сообщество пока не пересмотрело клинические рекомендации и не внедрило эти методы в рутинную практику. Возможно, это изменится, когда появятся более эффективные и безопасные противовоспалительные препараты.
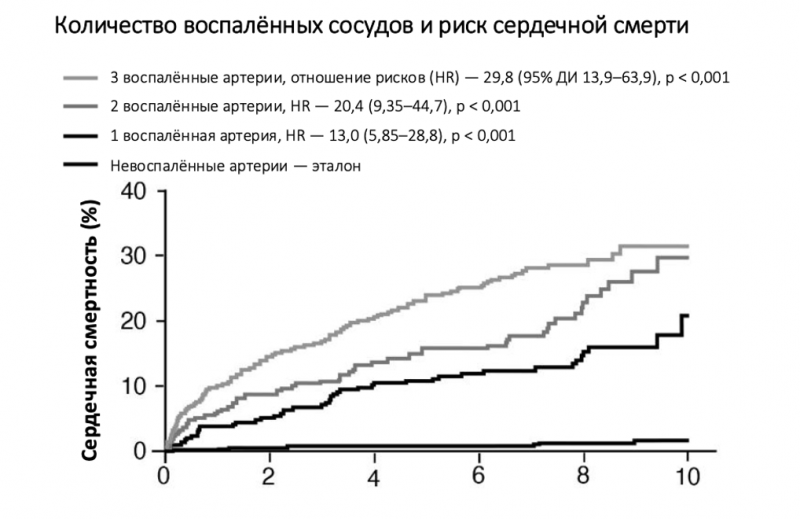
Рисунок 8. Взаимосвязь воспаления коронарных артерий (по данным КТ) и сердечной смертности. Адаптировано из Kenneth Chan et al., “Inflammatory Risk and Cardiovascular Events in Patients Without Obstructive Coronary Artery Disease: The ORFAN Study,” Lancet, 2024.
ПРОГНОЗИРОВАНИЕ И ПРОФИЛАКТИКА
Длительный период развития атеросклероза открывает уникальную возможность для раннего выявления людей с высоким риском ишемической болезни сердца, тщательного наблюдения за ними и своевременного вмешательства для коррекции факторов риска. Сегодня мы понимаем, что оценка риска должна выходить далеко за пределы традиционных клинических показателей — таких как диабет, ожирение, курение, малоподвижный образ жизни и повышенный уровень ЛПНП-холестерина (рисунок 9).
Современные данные о воспалении сердца добавляют новый уровень точности в прогнозирование и позволяют лучше выявлять тех, кто подвержен сердечно-сосудистым заболеваниям.
Помимо классических факторов, существует широкий спектр новых биомаркеров и технологий, способных выявить пациентов из группы высокого риска. В их число входят полигенные индексы, характеристики микробиома и протеома, «эпигенетические часы» — показатели метилирования ДНК, отражающие ускоренное старение организма, а также CHIP (клональная гематопоэзия с индуцированной мутацией). Биомаркеры воспаления, например высокочувствительный С-реактивный белок (вч-СРБ), дополняют картину.

Рисунок 9. Профилактика ишемической болезни сердца. Мультимодальный подход ИИ для выявления лиц с высоким риском, их активного наблюдения и агрессивных мер по блокированию прогрессирования атеросклероза и воспаления.
Новые методы так называемой «оппортунистической медицинской визуализации» — фотография сетчатки и рентгенография грудной клетки — позволяют выявлять признаки сердечно-сосудистого риска, хотя изначально эти обследования назначаются по другим причинам. Современные алгоритмы искусственного интеллекта способны точно оценивать кальциноз коронарных артерий и прогнозировать вероятность инфарктов и инсультов, анализируя именно эти изображения [70-71].
Выявление лиц из группы высокого риска — мультимодальный подход:
• Клинические факторы и история болезни
• КТ-коронарная ангиография
• Лабораторные показатели и динамика биомаркеров
• Полигенные и протеомные профили
• Микробиомные показатели риска
• Эпигенетические часы
• Вч-СРБ и другие маркеры воспаления
• Искусственный интеллект для анализа медицинских изображений (фотография сетчатки, рентгенография грудной клетки)
• Анализ образа жизни и факторов окружающей среды
Как только пациент определяется как находящийся в группе высокого риска, ему предлагается комплексный план активного наблюдения и раннего вмешательства. Важно стремиться к строгому контролю артериального давления — оптимальным считается уровень ниже 120 мм рт. ст., что подтверждено крупными рандомизированными исследованиями и снижает риск серьёзных сосудистых событий.
Высокоинтенсивная терапия статинами остаётся краеугольным камнем лечения. Если при этом сохраняются признаки воспаления, может быть оправдано применение противовоспалительных препаратов, таких как колхицин. В перспективе ожидается появление более эффективных средств, а также методов модуляции кишечного микробиома — нового направления в профилактике и терапии атеросклероза.
Все эти усилия отражают понимание воспаления как ключевого драйвера сердечно-сосудистых заболеваний и необходимость его подавления на ранних этапах, в течение длительного периода, предшествующего развитию клинических проявлений атеросклероза. Хотя в настоящее время такие подходы ещё не вошли в повседневную практику, именно они открывают путь к значительному снижению заболеваемости и смертности от ишемической болезни сердца — одного из главных возрастных заболеваний современности.
ФИБРИЛЛЯЦИЯ ПРЕДСЕРДИЙ
Существует ещё одно сердечно-сосудистое заболевание, тесно связанное с возрастом, но при этом более распространённое, сильнее обусловленное наследственностью и гораздо более поддающееся профилактике, чем принято считать. Фибрилляция предсердий (ФП) — это нарушение сердечного ритма, которое представляет собой ведущую причину эмболического инсульта, увеличивая его риск в пять раз. Этим заболеванием страдают более 60 миллионов человек по всему миру.
Возраст — главный фактор риска. Если у тридцатилетних вероятность развития ФП составляет всего 0,2%, то у людей старше 70 лет она достигает 4%. Пожизненный риск фибрилляции предсердий для взрослых старше 45 лет приближается к 25%. Помимо инсульта, это нарушение связано с повышенным риском развития сердечной недостаточности и увеличенной смертностью. Ожидаемая потеря продолжительности жизни после постановки диагноза в возрасте до 50 лет составляет в среднем 9 лет, а в возрасте 70 лет — около 5,4 года [72,73].
Многие факторы риска фибрилляции предсердий пересекаются с таковыми при атеросклеротических сердечно-сосудистых заболеваниях: возраст, ожирение, гипертония, диабет, курение, малоподвижный образ жизни и загрязнение воздуха. Но есть и более специфические предрасполагающие условия: обструктивное апноэ сна и другие нарушения сна, заболевания щитовидной железы и почек, хроническая обструктивная болезнь лёгких, психические расстройства, заболевания пародонта, а также избыточное потребление сладких напитков. У пожилых мужчин также выявлена связь с повышенным уровнем тестостерона. Повышенному риску подвержены и высокорослые люди, а также молодые элитные спортсмены, особенно при экстремальных нагрузках на выносливость [74,75].
Широко распространённый миф — будто кофеин способствует развитию фибрилляции предсердий. На самом деле, по данным многочисленных исследований, умеренное потребление кофеина ассоциируется скорее с сниженным риском возникновения этого нарушения ритма [76,77].
Рандомизированные клинические испытания показали, что снижение массы тела у пациентов с избыточным весом и ожирением существенно уменьшает частоту рецидивов фибрилляции и выраженность симптомов [78,79].
Как и ишемическая болезнь сердца, фибрилляция предсердий часто протекает бессимптомно. От 10 до 20% случаев остаются нераспознанными. Однако за последние годы возможности выявления этого состояния значительно улучшились — благодаря интеграции алгоритмов искусственного интеллекта в носимые устройства: «умные» часы и портативные сенсоры, закрепляемые на пальце, способны записывать одноканальную электрокардиограмму в момент, когда человек ощущает возможное нарушение ритма [81,81].
ГЕНЕТИКА, ВОСПАЛЕНИЕ И ПРОГНОЗИРОВАНИЕ ФИБРИЛЛЯЦИИ ПРЕДСЕРДИЙ
Мы не можем изменить свой возраст, рост или наследственность. Но мы можем оценить свой генетический риск — с помощью полигенного показателя риска (ППР). Уже выявлено более ста генетических локусов, ассоциированных с повышенной вероятностью развития фибрилляции предсердий (ФП). Согласно исследованию, проведённому в Mass General Brigham, более 8% пациентов имели высокий ППР — и этот риск удваивался вне зависимости от этнической принадлежности: у белых, чёрных и азиатских пациентов [82].
В масштабном исследовании с участием 25 000 взрослых участников, находящихся в верхних 3% по уровню ППР, было зарегистрировано двукратное увеличение риска развития ФП — в самых разных популяционных группах. Полигенные показатели также позволяют прогнозировать вероятность инсульта, вызванного фибрилляцией предсердий [83,84].
Роль воспаления подтверждается и другими маркерами. Повышенные уровни высокочувствительного С-реактивного белка (вч-СРБ), интерлейкина-6, фактора некроза опухоли (ФНО), а также мозгового натрийуретического пептида (BNP) связаны с повышенным риском ФП. Это созвучно с данными, указывающими на взаимосвязь между воспалительными заболеваниями, такими как пародонтоз, и сердечно-сосудистыми рисками [85,86].
К числу новых прогностических подходов можно отнести и так называемые «протеомные часы старения сердца» — биомаркеры, отражающие физиологический износ сердечной ткани [87,88].
Неожиданно, но весьма обнадёживающе, препараты GLP-1, изначально разработанные для лечения диабета и ожирения, в ходе крупных рандомизированных исследований продемонстрировали не только выраженный противовоспалительный эффект и снижение массы тела, но и снижение риска развития фибрилляции предсердий [89,90].
Добавим к этому эпигенетические маркеры, основанные на анализе метилирования ДНК: они тоже способны выявлять людей с повышенной предрасположенностью к ФП [91,92].
И всё же печальный парадокс: ни один из этих «омиксных» методов — ни полигенные, ни эпигенетические, ни протеомные тесты — пока не вошёл в повседневную клиническую практику. Их прогностическая ценность очевидна, но они по-прежнему остаются инструментами исследований, а не рутины.
В то же время искусственный интеллект уже способен извлекать прогностическую информацию из обычной 12-отведённой ЭКГ, записанной у пациента, никогда ранее не имевшего аритмий. Такие алгоритмы могут предсказать риск развития ФП и инсульта задолго до появления симптомов [93,94].
Что же касается вторичной профилактики, то здесь медицина располагает высокоэффективными средствами: антикоагулянты (разжижители крови) снижают риск инсульта у пациентов с установленной ФП и высоким тромбоэмболическим риском [95,96].
Между ишемической болезнью сердца и фибрилляцией предсердий проходит общая нить. Это — заболевания старения, тихо развивающиеся у миллионов людей, зачастую бессимптомно. Большинство из них даже не подозревает о своём риске. Но, вооружённые генетическими, эпигенетическими и воспалительными маркерами, мы уже знаем, как точно определять таких людей — и как вовремя вмешиваться.
Таким образом, мы уже располагаем знаниями и инструментами для профилактики самых важных сердечно-сосудистых заболеваний старения — и тем самым для продления здоровой жизни. Но всё ещё не используем их в полной мере.
СПИСОК ИСПОЛЬЗОВАННОЙ ЛИТЕРАТУРЫ
- World Health Organization. (2021). Cardiovascular diseases (CVDs).
- Baigent, C., Keech, A., Kearney, P. M., et al. (2005). “Efficacy and safety of cholesterol-lowering treatment: prospective meta-analysis of data from 90,056 participants in 14 randomised trials of statins.” The Lancet, 366(9493), 1267-1278.
- Farshidi, A., et al. (2022). “Effective Dose of Statin Post-PCI.” Interventional Cardiology Review, 17, e17.
- Rippe, J. M. (2019). “Lifestyle Strategies for Risk Factor Reduction, Prevention, and Treatment of Cardiovascular Disease.” American Journal of Lifestyle Medicine, 13(6), 552-568.
- Kolesnik, E., et al. (2022). “Hypertension as a risk factor for atherosclerosis: Cardiovascular risk and prevention.” Frontiers in Cardiovascular Medicine, 9, 9441708.
- MSD Manuals. (2024). “Atherosclerosis - Cardiovascular Disorders.”
- Pan, H., et al. (2024). “Atherosclerosis Is a Smooth Muscle Cell–Driven Tumor-Like Disease.” Circulation, 149(19), 1477–1494.
- Vanderbilt University Medical Center. (2024). “Cancer-Like Features in Atherosclerosis Provide New Opportunity for Treatment.” Inside Precision Medicine.
- Meijers, W. C., & de Boer, R. A. (2016). Shared risk factors in cardiovascular disease and cancer. Circulation, 133(11), 1104–1114.
- Smith, M. S. (2023). Ask the expert: What can we learn from links between cancer and cardiovascular disease? MSU Today.
- Conrad, N., et al. (2022). Autoimmune diseases and cardiovascular risk: a population-based study. The Lancet, 400(10354), 733–743.
- Meier, C. R., et al. (2022). Autoimmune disorders increase risk of cardiovascular disease. The Lancet.
- Mortensen, M. B., Fuster, V., Muntendam, P., et al. (2023). Subclinical Coronary Atherosclerosis and Risk for Myocardial Infarction in a Danish Population. Annals of Internal Medicine, 176(4), 513–522.
- American Heart Association. (2021). Life’s Essential 8: Key to Cardiovascular Health.
- Sharma, S., et al. (2019). Coronary Artery Disease in Young Adults: A Hard Lesson for Cardiovascular Health. Journal of the American College of Cardiology, 74(15), 1879–1882.
- Torkamani, A., et al. (2023). A multi-ancestry polygenic risk score improves risk prediction for coronary artery disease. Nature Medicine, 29, 1454–1464.
- Khera, A. V., Chaffin, M., Aragam, K. G., et al. (2020). Validation of a Genome-Wide Polygenic Score for Coronary Artery Disease in South Asians. Journal of the American College of Cardiology, 76(6), 703–714.
- Natarajan, P., et al. (2023). A multi-ancestry polygenic risk score improves risk prediction for coronary artery disease. Nature Medicine, 29, 1454–1464.
- Inouye, M., Abraham, G., Nelson, C. P., Wood, A. M., Sweeting, M. J., Dudbridge, F., … & Samani, N. J. (2018). Genomic risk prediction of coronary artery disease in 480,000 adults: Implications for primary prevention. Journal of the American College of Cardiology, 72(16), 1883–1893.
- Mars, N., Koskela, J. T., Ripatti, P., Kiiskinen, T. T. J., Havulinna, A. S., Lindbohm, J. V., … & Ripatti, S. (2020). Polygenic and clinical risk scores and their impact on age at onset and prediction of cardiometabolic diseases and common cancers. Nature Medicine, 26(4), 549–557.
- Lu, X., et al. (2023). A polygenic risk score improves risk stratification of coronary artery disease: a large-scale prospective Chinese cohort study. European Heart Journal, 43, 1519–1531.
- Williams, M. J., et al. (2024). Proteomic analysis of cardiorespiratory fitness for prediction of clinical outcomes. Nature Medicine, 30, 1234–1245.
- Lehallier, B., Williams, M. J., et al. (2024). Proteomic aging clock predicts mortality and risk of common age-related diseases. Nature Aging, 4, 678–691.
- Williams, M. J., et al. (2024). Proteomic aging clock (PAC) predicts age-related outcomes in the general population. Aging Cell, 23(4), e14023.
- Sundström, J., et al. (2024). Markers of imminent myocardial infarction. Nature Cardiovascular Research. https://doi.org/10.1038/s44161-024-00422-2
- Fidler, T. P., et al. (2023). Clonal Hematopoiesis of Indeterminate Potential From a Heart Failure Perspective. Journal of the American Heart Association, 12(15), e030603.
- Pascual-Figal, D. A., et al. (2023). Clonal Hematopoiesis of Indeterminate Potential Predicts Adverse Outcomes in Atherosclerotic Cardiovascular Disease. Journal of the American College of Cardiology, 81(19), 1919–1931.
- Suzhou Cardiometabolic Health Study Group. (2025). Advancing early detection of organ damage and cardiovascular risk: integrating oral microbiota and metabolic factors in a prospective cohort of 5,000–6,000 participants. Frontiers in Endocrinology, 16, Article 1522756.
- Bender, D., et al. (2021). Dietary interventions reduce traditional and novel cardiovascular risk markers via modulation of gut microbiome composition and metabolites: a randomized controlled trial. Frontiers in Cardiovascular Medicine, 8, 691564.
- Li, C., Stražar, M., Mohamed, A. M. T., et al. (2024). Gut microbiome and metabolome profiling in Framingham Heart Study reveals cholesterol-metabolizing bacteria. Cell, 186(7), 1500–1514.e15. https://doi.org/10.1016/j.cell.2024.03.014
- Fernández-Ruiz, I. (2024). Gut bacteria can break down cholesterol. Nature Reviews Cardiology, 21, 357. https://doi.org/10.1038/s41569-024-01026-w
- Wilmanski, T., Diener, C., Rappaport, N., Patwardhan, S., Wiedrick, J., Lapidus, J., Earls, J. C., Zimmer, A., Glusman, G., Robinson, M., Yurkovich, J. T., Kado, D. M., Cauley, J. A., Zmuda, J. M., & Price, N. D. (2021). Gut microbiome pattern reflects healthy ageing and predicts survival in humans. Nature Metabolism, 3(2), 274–286. https://doi.org/10.1038/s42255-021-00348-0
- Claesson, M. J., Jeffery, I. B., Conde, S., Power, S. E., O’Connor, E. M., Cusack, S., Harris, H. M., Coakley, M., Lakshminarayanan, B., O’Sullivan, O., Fitzgerald, G. F., Deane, J., O’Connor, M., Harnedy, N., O’Connor, K., O’Mahony, D., van Sinderen, D., Wallace, M., Brennan, L., … & O’Toole, P. W. (2012). Gut microbiota composition correlates with diet and health in the elderly. Nature, 488(7410), 178–184. https://doi.org/10.1038/nature11319
- Piperni, E., Nguyen, L. H., et al. (2024). Intestinal Blastocystis is linked to healthier diets and more favorable cardiometabolic outcomes in 56,989 individuals from 32 countries. Cell, 187(1), 1–18. https://doi.org/10.1016/j.cell.2024.03.014
- Nguyen, L. H., et al. (2024). A gut microbe could hold a key to help people benefit from healthy foods. Massachusetts General Hospital News. https://www.massgeneral.org/news/press-release/gut-microbe-help-people-benefit-eating-healthy-foods
- Blaha, M. J., Cainzos-Achirica, M., et al. (2023). When Does a Calcium Score Equate to Secondary Prevention? Journal of the American College of Cardiology: Cardiovascular Imaging, 16(9), 1395–1403.
- Detrano, R., Guerci, A. D., et al. (2008). Coronary calcium as a predictor of coronary events in four racial or ethnic groups. New England Journal of Medicine, 358(13), 1336–1345.
- Cannon, C. P., et al. (2015). Ezetimibe Added to Statin Therapy after Acute Coronary Syndromes. The IMPROVE-IT Trial.
- Sabatine, M. S., et al. (2017). Evolocumab and Clinical Outcomes in Patients with Cardiovascular Disease. The FOURIER Trial.
- Kim, J. H., & Kim, H. S. (2023). Optimal Target Low-density Lipoprotein Level for Reducing the Risk of Cardiovascular Disease and Its Recent Trends. Korean Journal of Clinical Pharmacology, 33(4), 270–277.
- Mach, F., Baigent, C., Catapano, A. L., et al. (2020). 2019 ESC/EAS Guidelines for the management of dyslipidaemias: lipid modification to reduce cardiovascular risk. European Heart Journal, 41(1), 111–188.
- Sattar, N., Preiss, D., Murray, H. M., et al. (2010). Statins and risk of incident diabetes: a collaborative meta-analysis of randomised statin trials. The Lancet, 375(9716), 735–742.
- Lee, S. H., et al. (2023). Rosuvastatin versus atorvastatin for prevention of cardiovascular events and new-onset diabetes mellitus in patients with coronary artery disease: results from the randomized LODESTAR trial. The BMJ, 382, e074485.
- Baptista, J. D., et al. (2021). Triglycerides and risk of atherosclerotic cardiovascular disease. Archives of Cardiovascular Diseases, 114(3), 197–206.
- Fan, W., Philip, S., Granowitz, C., Toth, P. P., & Wong, N. D. (2019). High Triglycerides Are Associated With Increased Cardiovascular Events, Medical Costs, and Resource Use: A Real-World Administrative Claims Analysis of Statin-Treated Patients. Journal of the American Heart Association, 8(15), e012742. https://doi.org/10.1161/JAHA.119.012742
- Bhatt, D. L., Steg, P. G., Miller, M., et al. (2019). Reduction in Cardiovascular Events with Icosapent Ethyl for Hypertriglyceridemia. New England Journal of Medicine, 380(1), 11–22. https://doi.org/10.1056/NEJMoa1812792
- Manson, J. E., Cook, N. R., Lee, I. M., et al. (2019). Marine n−3 Fatty Acids and Prevention of Cardiovascular Disease and Cancer. New England Journal of Medicine, 380(1), 23–32. https://doi.org/10.1056/NEJMoa1811403
- Raal, F. J., Rosenson, R. S., Reeskamp, L. F., et al. (2020). Evinacumab for Homozygous Familial Hypercholesterolemia. New England Journal of Medicine, 383(8), 711–720. https://doi.org/10.1056/NEJMoa2004215
- Santos, R. D., Rader, D. J., Cuchel, M., et al. (2024). Evinacumab for Pediatric Patients With Homozygous Familial Hypercholesterolemia. Circulation, 149(5), 343–353. https://doi.org/10.1161/CIRCULATIONAHA.123.065529
- Raal, F. J., et al. (2024). Zodasiran, an RNAi Therapeutic Targeting ANGPTL3, for Mixed Hyperlipidemia: Results from a Phase 2b Trial. New England Journal of Medicine, 390(11), 1023–1033. https://doi.org/10.1056/NEJMoa2401234
- Alexander, V. J., et al. (2025). Effect of Plozasiran, an RNAi Therapeutic Targeting Apolipoprotein C-III, on Lipoprotein Particle Profiles in Patients with Mixed Hyperlipidemia. Journal of the American College of Cardiology, 85(10), 1125–1136. https://doi.org/10.1016/j.jacc.2025.03.496
- Madsen, C. M., Varbo, A., Nordestgaard, B. G. (2018). Extreme high high-density lipoprotein cholesterol is paradoxically associated with high mortality in men and women: two prospective cohort studies. European Heart Journal, 39(27), 2478–2486. https://doi.org/10.1093/eurheartj/ehx163
- 52. Ko, D. T., Alter, D. A., Guo, H., et al. (2016). High-density lipoprotein cholesterol and cause-specific mortality in individuals without previous cardiovascular conditions: the CANHEART study. Journal of the American College of Cardiology, 68(19), 2073–2083. https://doi.org/10.1016/j.jacc.2016.08.038
- Ballantyne, C. M., & Laufs, U. (2020). Low-density lipoprotein cholesterol, high-density lipoprotein cholesterol, and triglycerides: Current knowledge and future directions for lipid management. European Heart Journal Supplements, 22(Supplement_E), E1-E9. https://doi.org/10.1093/eurheartj/suaa109
- Goff, D. C., Lloyd-Jones, D. M., Bennett, G., et al. (2014). 2013 ACC/AHA Guideline on the Assessment of Cardiovascular Risk: A Report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines. Journal of the American College of Cardiology, 63(25 Pt B), 2935–2959. https://doi.org/10.1016/j.jacc.2013.11.005
- Tsimikas, S., et al. (2022). Lipoprotein(a) in atherosclerotic cardiovascular disease and aortic stenosis: a European Atherosclerosis Society consensus statement. European Heart Journal, 43(39), 3925–3946. https://doi.org/10.1093/eurheartj/ehac361
- Rocha, N. A., et al. (2023). Lipoprotein(a) Testing Trends in a Large Academic Health System. Journal of the American Heart Association, 12(18), e031255. https://doi.org/10.1161/JAHA.123.031255
- Nissen, S. E., Wolski, K., Balog, C., et al. (2024). Recent updates on therapeutic targeting of lipoprotein(a) with RNA interference. Current Opinion in Lipidology, 35(4), 197–204. https://doi.org/10.1097/MOL.0000000000000922
- Sniderman, A. D., Thanassoulis, G., Glavinovic, T., et al. (2022). Apolipoprotein B Particles and Cardiovascular Disease: A Narrative Review. Journal of the American Heart Association, 11(20), e025858. https://doi.org/10.1161/JAHA.122.025858
- Ference, B. A., & Catapano, A. L. (2020). Beyond LDL-C: unravelling the residual atherosclerotic cardiovascular disease risk. Frontiers in Cardiovascular Medicine, 11, 1389106 (2024). https://doi.org/10.3389/fcvm.2024.1389106
- Sniderman, A. D., Thanassoulis, G., Glavinovic, T., et al. (2023). Use of Apolipoprotein B in the Era of Precision Medicine: Time for a Paradigm Change? Current Atherosclerosis Reports, 25, 793–804. https://doi.org/10.1007/s11883-023-01152-9
- Welsh, C., & Sattar, N. (2024). Discordance among apoB, non–high-density lipoprotein cholesterol, and LDL cholesterol: implications for cardiovascular risk assessment. European Heart Journal, 45(27), 2410–2418. https://doi.org/10.1093/eurheartj/ehad456
- Ridker, P. M., Everett, B. M., Thuren, T., et al. (2017). Antiinflammatory Therapy with Canakinumab for Atherosclerotic Disease. New England Journal of Medicine, 377(12), 1119–1131. https://doi.org/10.1056/NEJMoa1707914
- ACC.org: Canakinumab Anti-Inflammatory Thrombosis Outcomes Study (CANTOS) American College of Cardiology. https://www.acc.org/Latest-in-Cardiology/Clinical-Trials/2017/08/26/08/35/CANTOS
- Ridker, P. M., MacFadyen, J. G., Thuren, T., et al. (2017). Effect of Interleukin-1β Inhibition with Canakinumab on Incident Lung Cancer in Patients with Atherosclerosis: Exploratory Analysis of a Randomised, Double-Blind, Placebo-Controlled Trial. The Lancet, 390(10105), 1833–1842. https://doi.org/10.1016/S0140-6736(17)32247-X
- Tardif, J. C., Kouz, S., Waters, D. D., et al. (2019). Efficacy and Safety of Low-Dose Colchicine after Myocardial Infarction. New England Journal of Medicine, 381(26), 2497–2505. https://doi.org/10.1056/NEJMoa1912388
- Nidorf, S. M., Fiolet, A. T. L., Eikelboom, J. W., et al. (2020). Colchicine in Patients with Chronic Coronary Disease. New England Journal of Medicine, 383(19), 1838–1847. https://doi.org/10.1056/NEJMoa2021372
- Nidorf, S. M., Fiolet, A. T. L., Eikelboom, J. W., et al. (2020). Colchicine in Patients with Chronic Coronary Disease. New England Journal of Medicine, 383(19), 1838–1847. https://doi.org/10.1056/NEJMoa2021372
- Aung, N., et al. (2023). Drivers of mortality in patients with chronic coronary disease in the Low-Dose Colchicine 2 (LoDoCo2) trial.
- Hu, W., Zhu, L. Z., & colleagues. (2025). Could AI eye scans help doctors identify heart disease and stroke risk? npj Digital Medicine. Centre for Eye Research Australia. Available at: https://www.cera.org.au/could-ai-eye-scans-help-doctors-identify-heart-disease-and-stroke-risk/
- Weiss, J., et al. (2024). Opportunistic Screening for Cardiovascular Risk Using Deep Learning on Chest Radiographs. Circulation, 150(Suppl_1), A4138647.
- Deif, B., Lowres, N., Freedman, B. (2012). Prevalence of atrial fibrillation in the general population and in high risk groups: the Euro Heart Survey. Europace, 14(11), 1553–1559.
- Nielsen, P. B., Larsen, T. B., Gorst-Rasmussen, A., Overvad, T. F., Lip, G. Y. H., & Skjøth, F. (2024). Atrial fibrillation: age at diagnosis, incident cardiovascular events, and mortality—a nationwide population-based cohort study. European Heart Journal, 45(24), 2119–2130.
- Chugh, S. S., Havmoeller, R., Narayanan, K., Singh, D., Rienstra, M., Benjamin, E. J., Gillum, R. F., Kim, Y. H., McAnulty, J. H., Jr, Zheng, Z. J., Fornage, M., Nair, V., Kolodgie, F. D., & others. (2014). Worldwide Epidemiology of Atrial Fibrillation: A Global Burden of Disease 2010 Study. Circulation, 129(8), 837–847. doi:10.1161/CIRCULATIONAHA.113.005119
- Benjamin, E. J., Wolf, P. A., D’Agostino, R. B., Silbershatz, H., Kannel, W. B., & Levy, D. (1994). Impact of Atrial Fibrillation on the Risk of Death: The Framingham Heart Study. Circulation, 98(10), 946–952. doi:10.1161/01.CIR.98.10.946
- Cheng, M., Hu, Z., Lu, X., Huang, J., & Gu, D. (2022). Association of Coffee Consumption With Atrial Fibrillation Risk: A Dose–Response Meta-Analysis of Prospective Cohort Studies. Frontiers in Cardiovascular Medicine, 9, 894664. doi:10.3389/fcvm.2022.894664
- Larsson, S. C., Drca, N., & Wolk, A. (2013). Caffeine does not increase the risk of atrial fibrillation: a systematic review and meta-analysis of observational studies. Heart, 99(22), 1383–1389. doi:10.1136/heartjnl-2013-303950
- Abed, H. S., Wittert, G. A., Leong, D. P., Shirazi, M. G., Bahrami, B., Middeldorp, M. E., Lorimer, M. F., Lau, D. H., Antic, N. A., Brooks, A. G., Abhayaratna, W. P., Kalman, J. M., & Sanders, P. (2013). Effect of Weight Reduction and Cardiometabolic Risk Factor Management on Symptom Burden and Severity in Patients With Atrial Fibrillation: A Randomized Clinical Trial. JAMA, 310(19), 2050–2060. doi:10.1001/jama.2013.280521
- Pathak, R. K., Middeldorp, M. E., Lau, D. H., Mehta, A. B., Mahajan, R., Twomey, D., Alasady, M., Hanley, L., Antic, N. A., McEvoy, R. D., Kalman, J. M., Abhayaratna, W. P., & Sanders, P. (2015). Long-Term Effect of Goal-Directed Weight Management in an Atrial Fibrillation Cohort: A Long-Term Follow-Up Study (LEGACY). Journal of the American College of Cardiology, 65(20), 2159–2169. doi:10.1016/j.jacc.2015.03.002
- Martínez-Sellés, M., Bueno, H., Dalli, E., Fernández-Ortiz, A., & Fernández-Pérez, C. (2013). Prevalence of Undiagnosed Atrial Fibrillation and of That Not Being Treated With Oral Anticoagulants. Revista Española de Cardiología (English Edition), 66(3), 205–212. doi:10.1016/j.1885-5857(13)70006-X
- Ponikowski, Z., Szymański, M., Dziuda, Ł., et al. (2024). Artificial intelligence-enabled atrial fibrillation detection using smartwatches. Current Cardiology Reports, 26(7), epub ahead of print. doi:10.1007/s11886-024-02072-6
- Roselli, C., Chaffin, M. D., Weng, L.-C., et al. (2025). Multi-ancestry genome-wide association study of atrial fibrillation reveals new insights into biology and risk prediction. Nature Genetics, 57(3), 330–341. doi:10.1038/s41588-024-02072-3
- Vad, O. B., Monfort, L. M., Paludan-Müller, C., et al. (2024). Rare and Common Genetic Variation Underlying Atrial Fibrillation Risk. JAMA Cardiology, 9(8), 732–740. doi:10.1001/jamacardio.2024.1528
- Khurshid, S., Weng, L.-C., Al-Alusi, M. A., et al. (2021). Combining Clinical and Polygenic Risk Improves Stroke Prediction in Atrial Fibrillation. Circulation: Genomic and Precision Medicine, 14(4), e003168. doi:10.1161/CIRCGEN.120.003168
- Rydén, L., Buhlin, K., Ekstrand, E., et al. (2016). Periodontal Disease and Cardiovascular Disease: A Literature Review. Circulation, 133(6), 576-583. doi:10.1161/CIRCULATIONAHA.115.020869
- Naqvi, T. Z., Lee, M.-S., & others. (2020). Inflammation and Circulating Natriuretic Peptide Levels. Circulation Research, 126(1), 72-85. doi:10.1161/CIRCRESAHA.119.315909
- Oh, H. S.-H., Rutledge, J., Nachun, D., et al. (2023). Organ aging signatures in the plasma proteome track health and disease. Nature, 623(7986), 164–172. doi:10.1038/s41586-023-06802-1
- Argentieri, M. A., Chen, Z., Burgess, S., et al. (2024). Proteomic aging clock predicts mortality and risk of common age-related diseases in diverse populations. Nature Medicine, 30(8), 2314–2325. doi:10.1038/s41591-024-03164-7
- TRANSFORM-AF Investigators. (2025). Glucagon-like peptide-1 receptor agonists for secondary prevention of atrial fibrillation in patients with obesity: Results from the TRANSFORM-AF trial. Presented at Heart Rhythm 2025, San Diego, CA.
- Krychtiuk, M. A., et al. (2025). Glucagon-like peptide-1 analogues and prevention of atrial fibrillation: Insights from the HARMONY Outcomes trial and meta-analysis. European Journal of Preventive Cardiology. doi:10.1093/eurjpc/zwaf242
- Bressler, J., Fornage, M., Demerath, E. W., Knopman, D. S., Mosley, T. H., Boerwinkle, E., & Gottesman, R. F. (2021). Epigenetic Age and the Risk of Incident Atrial Fibrillation. Circulation, 144(24), 1899–1911. doi:10.1161/CIRCULATIONAHA.121.056456
- Gao, H., Li, J., Ma, Q., Zhang, Q., Li, M., Hu, X., & others. (2024). Causal Associations of DNA Methylation and Cardiovascular Disease: A Two-Sample Mendelian Randomization Study. Global Heart, 19(1), 1324. doi:10.5334/gh.1324
- Chen, Y.-H., Lin, Y.-J., et al. (2025). Utilizing 12-lead electrocardiogram and machine learning to predict atrial fibrillation and stroke risk. The Lancet Digital Health, 7(3), e198–e207. doi:10.1016/S2589-7500(24)00254-8
- Hughes, J. W., Khurshid, S., et al. (2022). ECG-Based Deep Learning and Clinical Risk Factors to Predict Atrial Fibrillation. Circulation, 145(15), 1228–1238. doi:10.1161/CIRCULATIONAHA.121.057480
- Doherty, J. U., Gluckman, T. J., Hucker, W. J., Januzzi, J. L., Ortel, T. L., Saxonhouse, S. J., & Spinler, S. A. (2022). Direct Oral Anticoagulants Versus Warfarin in Patients With Atrial Fibrillation. Circulation, 145(8), 626–636. doi:10.1161/CIRCULATIONAHA.121.056355
- Hart, R. G., Pearce, L. A., Aguilar, M. I. (2007). Meta-analysis: Antithrombotic Therapy to Prevent Stroke in Patients Who Have Nonvalvular Atrial Fibrillation. Annals of Internal Medicine, 146(12), 857–867. doi:10.7326/0003-4819-146-12-200706190-00007